Magnetresonanztomographie (MRT) ▷ Ablauf, Kosten, Sicherheit und Funktionsweise
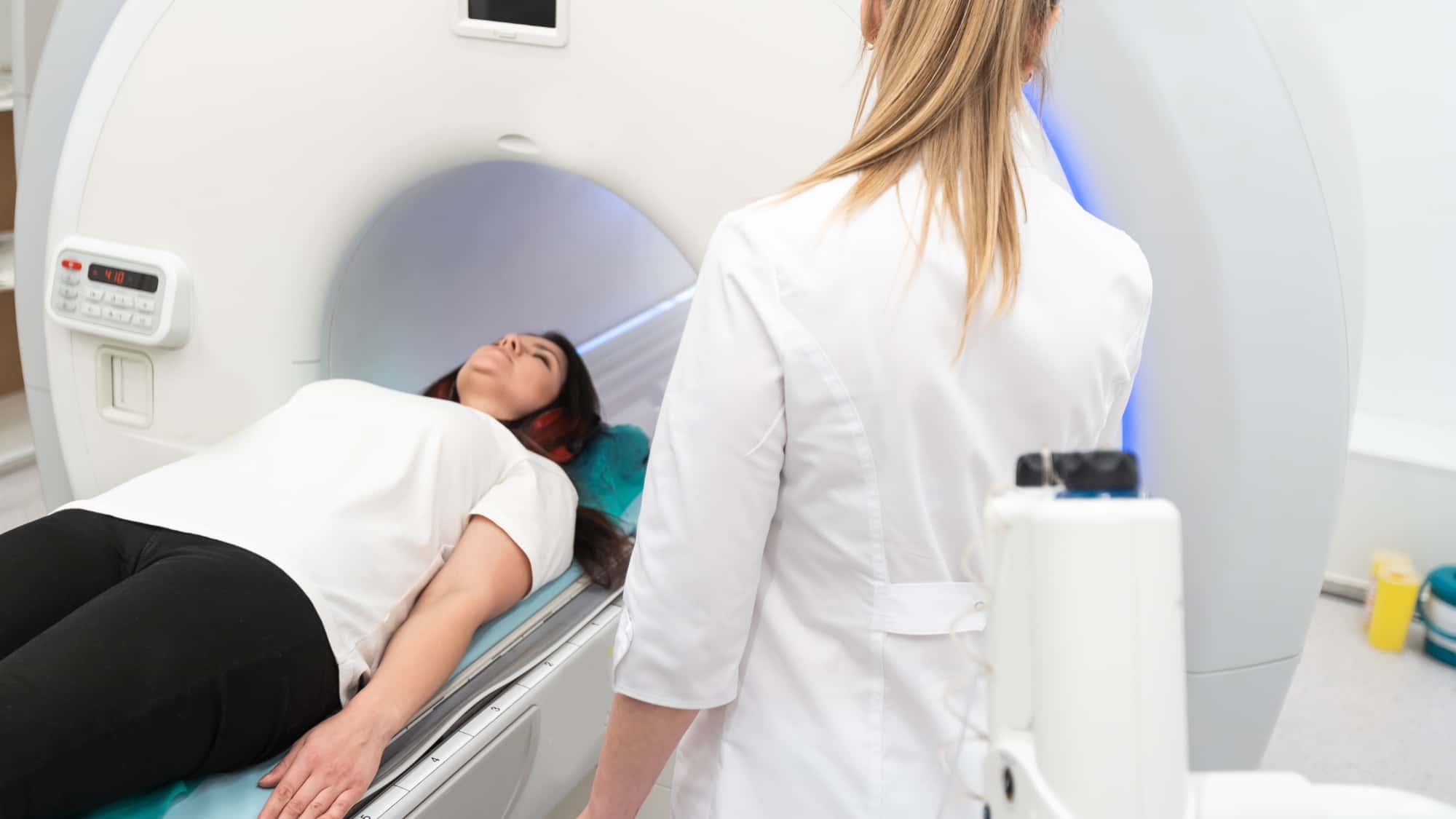
Die MRT ist eines der wichtigsten schmerzfreien Bildgebungsverfahren der Medizin (Foto: Andrew Angelov | Shutterstock)
In diesem Artikel:
- Was ist eine MRT?
- Ablauf
- Was sieht man bei der Kernspintomographie?
- Ist eine Kernspintomographie gefährlich?
- MRT-Untersuchungen trotz Platzangst?
- MRT in der Schlaganfall-Diagnostik
- Kosten
- Praxis-Tipps
Das Wichtigste in Kürze:
- Die auch als Kernspintomographie bezeichnete Magnetresonanztomographie, kurz MRT, stellt neben der Computertomographie (CT) eines der wichtigsten schmerzfreien Bildgebungsverfahren der Medizin, insbesondere der Neurologie, dar.
- Die MRT erzeugt ohne den Einsatz ionisierender Röntgenstrahlung Schnittbilder von gewünschten Bereichen des menschlichen Körpers, die zu einem dreidimensionalen Bild zusammengefügt werden können. Sie nutzt Magnetfelder und beruht auf Eigenschaften der Wasserstoffatome, die im menschlichen Körper vorkommen.
- Vor allem für Untersuchungen des Schädels, insbesondere im Rahmen der Schlaganfall-Diagnostik, eignen sich kernspintomographische Untersuchungen aufgrund des hohen Weichteilkontrastes hervorragend.
- MRT-Untersuchungen sind in der Regel zeit- und kostenintensiver als vergleichbare CT-Untersuchungen, daher richtet sich die Wahl des Bildgebungsverfahrens grundsätzlich nach der medizinischen Fragestellung und nach der Krankenvorgeschichte des Patienten.
Was ist Magnetresonanztomographie (MRT)?
Die Kernspintomographie, auch Magnetresonanztomographie oder MRT genannt, ist neben der Computertomographie, kurz CT, ein weiteres relevantes medizinisches Bildgebungsverfahren, das zur Diagnosestellung auch im Bereich der Neurologie und hier insbesondere in der Diagnostik des Schlaganfalls eingesetzt wird.1
Die Zeit nach der Klinik ist für Angehörige oft die größte Herausforderung. Unser Online-Kurs führt Sie in 13 kompakten Modulen durch die Zeit danach. Der Kurs ist ein kostenfreies Angebot gesetzlicher Krankenkassen nach § 45 SGB XI.
Wie läuft eine Kernspintomographie-Untersuchung ab?
Das Aufklärungsgespräch
Bevor die Untersuchung mittels Magnetresonanztomographie erfolgt, findet üblicherweise ein Aufklärungsgespräch mit dem Radiologen beziehungsweise Neuroradiologen statt. Der Radiologe ist ein Facharzt für bildgebende Diagnostik. Beschäftigt er sich speziell mit dem menschlichen Nervensystem, spricht man von einem Neuroradiologen.
Das Aufklärungsgespräch hat zum Zweck, dass Patientinnen und Patienten etwaige Fragen klären und ihre Krankenvorgeschichte in Bezug auf die bevorstehende Untersuchung mit dem Arzt besprechen können. Besonders Herzschrittmacher oder Implantate des Patienten können Gegenstand des Aufklärungsgesprächs sein, da unter Umständen bestimmte Vorsichtsmaßnahmen erforderlich sein können oder die MRT als Untersuchungsmethode ausgeschlossen werden muss.
Ziel des Gesprächs ist die umfassende Aufklärung der Patientinnen und Patienten über den Ablauf der Untersuchung, mögliche Risiken und je nach Fragestellung die Notwendigkeit der Verabreichung eines Kontrastmittels. Da eine intakte Nierenfunktion die Grundlage für den Einsatz von Kontrastmitteln darstellt, werden aktuelle Blutuntersuchungs-Befunde in die Planung des weiteren Vorgehens einbezogen und gegebenenfalls vor der MRT-Untersuchung noch eine Blutuntersuchung zur Ermittlung der für die Nierenfunktion relevanten Blutparameter angeordnet.8
Weiterhin dient es dem behandelnden Arzt zur Abwägung von Nutzen und Risiko der Untersuchung und der Einschätzung, ob weitere Voruntersuchungen erforderlich sind beziehungsweise ob alternative diagnostische Methoden eingesetzt werden können, wenn die MRT aus bestimmten Gründen nicht in Frage kommt.
Wenn alle Fragen und Bedenken des Patienten geklärt wurden und der Arzt zu der Entscheidung kommt, dass die medizinische Fragestellung mittels Kernspintomographie bestmöglich beantwortet werden kann, wird ein Termin für die eigentliche Untersuchung geplant.
Die kernspintomographische Untersuchung
Bevor die Untersuchung stattfinden kann, werden Patientinnen und Patienten gebeten, alle metallhaltigen Gegenstände wie zum Beispiel Uhren, Schmuck, Piercings und Brillen abzulegen. Auch metallhaltige Kleidung, u. a. Gürtel oder Hosen mit Metallknöpfen, wird vor der Untersuchung abgelegt. Grundsätzlich können Patientinnen und Patienten jedoch ihre Kleidung bei der Untersuchung anbehalten. Ergänzend wird empfohlen, zur Untersuchung ohne Make-up zu erscheinen, da dieses ebenfalls Metallpartikel enthalten kann.
Wenn alle gefährdenden Materialien im Nebenraum des Untersuchungsraumes abgelegt wurden, darf der Patient gemeinsam mit dem medizinischen Personal den Untersuchungsraum betreten und sich mit dem Kernspintomographen vertraut machen. Einige Patienten benötigen hierzu möglicherweise etwas mehr Zeit, wenn sie unter Platzangst leiden.
Bei ausgeprägter Platzangst kann ein Beruhigungsmittel verabreicht werden. Ein Grund zur Besorgnis besteht jedoch nicht. Sobald Patient und medizinisches Fachpersonal bereit sind, wird der Patient auf dem Untersuchungstisch gelagert. Die Art und Weise der Lagerung richtet sich nach dem zu untersuchenden Bereich. Gegebenenfalls kommen Kissen und Polster zum Einsatz, um eine ruhige und möglichst bequeme Lage zu gewährleisten.
Je nach Untersuchung wird möglicherweise eine MRT-Spule auf die zu untersuchende Körperregion aufgesetzt. Der Patient wird anschließend langsam vollständig oder nur zum Teil in die MRT-Röhre gefahren und im Magnetfeld positioniert. Wie weit der Patient mit Kopf oder Füßen voran in die Röhre gefahren wird, richtet sich nach dem zu untersuchenden Bereich. Die besten Bilder werden erzielt, indem der zu untersuchende Bereich in der Mitte der Röhre, dem sogenannten Isozentrum, liegt.
Der Innendurchmesser der MRT-Röhre beträgt etwa 70 Zentimeter. Die Untersuchung dauert in Abhängigkeit vom zu untersuchenden Gewebe oder Organ etwa zwischen zehn Minuten und einer Stunde.9 Eine Untersuchung des Schädels dauert etwa 30 Minuten und somit halb so lang wie die Untersuchung des gesamten Körpers.10 Für derartige Untersuchungen werden Patienten maximal mit dem Kopf voran bis zum Schultergürtel in die MRT-Röhre geschoben, der Rest des Körpers bleibt also hierbei außerhalb der Röhre.8
Während der Untersuchung kommt es zu “klopfenden” und “hämmernden” Geräuschen, daher erhalten Patienten vor Beginn der Untersuchung einen Gehörschutz. Die Untersuchung ist absolut ungefährlich und die nur in einzelnen Fällen eingesetzten Kontrastmittel sind in aller Regel gut verträglich. Für manche Untersuchungen kann es erforderlich sein, dass die Patienten für eine bestimmte Dauer keine Mahlzeiten zu sich nehmen. Dies wird dann im jeweiligen Einzelfall bereits im Aufklärungsgespräch besprochen.
Grundsätzlich stehen für die Untersuchung zwei verschiedene Arten von MR-Tomographen zur Verfügung:
- geschlossene MRT-Geräte
- offene MRT-Geräte
Die geschlossenen Tomographen sind diejenigen, die den meisten Patientinnen und Patienten bekannt sind. Sie sind bis zu 2,5 Meter lang und die Messung dauert in der Regel etwa zwischen 15 und 30 Minuten. Eine Überwachung durch das medizinische Personal erfolgt üblicherweise über einen Bildschirm im Nachbarraum für die gesamte Dauer der Untersuchung.
Offene Tomographen besitzen eine seitliche Öffnung und vor allem bei Patientinnen und Patienten mit Angst vor engen Räumen sehr beliebt. Allerdings ist bei diesen Geräten der Abstand zum Kopf durch den kleineren Innendurchmesser geringer und die Untersuchungsdauer länger.10
Die Befunderstellung und Besprechung
Die mit der Kernspintomographie gewonnenen Daten werden im sogenannten K-Raum, einem virtuellen Zwischenspeicher, gespeichert und verarbeitet, sodass die Bilder wenige Minuten nach Abschluss der Untersuchung zur Verfügung stehen.
In den meisten Fällen wird jedoch ein gesonderter Termin zur Befundbesprechung mit dem die Untersuchung leitenden (Neuro-)Radiologen oder dem überweisenden Arzt vereinbart, da die Bilder ausgewertet und beurteilt werden müssen. Im Rahmen der Befundbesprechung wird dann auch die weitere Vorgehensweise und gegebenenfalls Therapie besprochen.10
Was sieht man bei der Kernspintomographie und was nicht?
Die MRT erfreut sich immer größerer Beliebtheit als bildgebendes Verfahren, vor allem im Bereich der Neurologie. Es können sowohl wasserhaltige Gewebe, aber auch Fette und Proteine dargestellt werden, da diese sehr viele Wasserstoffatome aufweisen.3
Insbesondere im Bereich der Tumor-Diagnostik weicher Organe und der Diagnostik des Gehirns hat die Magnetresonanztomographie immense Bedeutung erlangt.
Die MR-Tomographie wird für vielseitige Untersuchungen unter anderem im Bereich des Schädels, im Hals-Nasen-Ohren-Bereich, am Herz-Kreislauf-System und am Bewegungsapparat eingesetzt. So können verschiedene Tumoren, Krankheiten des Nervensystems, Demenz, Erkrankungen des Rückenmarks, Blutungen und Hirninfarkte hervorragend untersucht werden.
Bei der Darstellung von Knochen und luftgefüllten Räumen wie etwa der Lunge stößt die MRT hingegen an ihre Grenzen, da diese einen geringen Wassergehalt haben und somit kaum Protonen vorhanden sind, die Grundlage für die magnetresonanztomographische Messung sind. Für die Untersuchung solcher Strukturen eignen sich röntgenbasierte Untersuchungen, wie etwa die Computertomographie, deutlich besser.
Bei dem gemessenen Signal handelt es sich um Magnetisierung. Grundsätzlich erscheinen kräftige Signale hyperintens oder hell, schwache Signale hypointens oder dunkel.
Sicherheitsaspekte der MRT-Untersuchung
Das größte Sicherheitsrisiko entsteht bei der MRT durch metallische Gegenstände, die vom Magneten angezogen werden. Um sicherzustellen, dass keine metallischen Gegenstände übersehen werden, die zu einer Gefährdung von Patient, Begleitperson oder Personal führen können, setzt man heutzutage häufig Schleusen mit Metall-Detektoren ein.
Eine besondere Gefahr besteht auch für Patientinnen und Patienten mit Herzschrittmachern, denn diese können durch das starke Magnetfeld in einen anderen Betriebszustand versetzt werden, was schlimmstenfalls lebensbedrohliche Folgen haben kann. Auch für Patienten mit Defibrillatoren, die durch elektrische Impulse das Herz bei erhöhter unregelmäßiger Herzfrequenz in den regelmäßigen Ausgangsrhythmus zurück versetzen können, ist der Einsatz der MRT nur nach strenger Abwägung der Risiken erlaubt.11
Implantate aus ferromagnetischem Material, bei dem sich die magnetischen Momente aller Atome in die gleiche Richtung, also parallel ausrichten, können ebenfalls durch das starke Magnetfeld der MRT-Anlage beeinflusst werden.11
Erhöhte Vorsicht ist geboten, wenn Patientinnen oder Patienten eisen- oder bleihaltige Tätowierungen, Zahnspangen, ältere Herzklappen, Metallplatten oder Piercings haben. Einige Tätowierungen können sich erwärmen und so zu schwersten Verbrennungen führen. Stark magnetische Bestandteile von Zahnspangen können beschädigt werden und bei Untersuchungen von Kopf und Halswirbelsäule zu diagnostischen Fehlbefunden führen, da diese die MRT stören. Ältere Metallplatten bestehen meist nicht aus dem für die MRT unbedenklichen Titan, sondern aus magnetischen Materialien. Piercings sollten vor der Untersuchung entfernt werden, da magnetisches Material zu Verletzungen führen könnte. Lediglich Piercings aus Titan und Edelstahl sind als unbedenklich einzustufen.
Eine Gefährdung geht weiterhin von Metallsplittern aus, da sie sich abhängig davon, wo sie sich befinden, erwärmen und dadurch bewegen können. Dies kann zu ernsthaften Verletzungen führen. Dennoch stellen Metallsplitter nicht grundsätzlich ein Hindernis dar.
Die Patientinnen und Patienten sollten zur Untersuchung mit Kleidung ohne metallische Reißverschlüsse und Knöpfe erscheinen. Zudem sollten keine Armbanduhren, mp3-Player, iPods, Mobiltelefone, Magnetkarten oder Schmuck mit in den Untersuchungsraum genommen werden. Auch Haarspangen müssen für die Untersuchung aus dem Haar genommen werden.
Insbesondere bei der Verabreichung von Kontrastmitteln kann es in seltenen Fällen zu Übelkeit oder allergischen Reaktionen kommen. Zudem muss auf eine intakte Nierenfunktion geachtet werden, da die Ausscheidung des Kontrastmittels über die Nieren erfolgt. Daher sollten vor der Untersuchung entsprechende Laborwerte bestimmt und bekannte Unverträglichkeiten abgeklärt werden.
Vor der Untersuchung wird bei Patientinnen das Vorliegen einer Schwangerschaft abgeklärt, die möglicherweise zum Zeitpunkt der Terminvereinbarung noch nicht bekannt war. In diesem Fall wird mit dem untersuchenden Arzt besprochen, ob die MRT durchgeführt werden kann.
Durch den Einsatz sehr starker Magnetfelder kann es beim Patienten zu Schwindelgefühlen und Augenflimmern kommen, jedoch haben diese keine schädliche Wirkung auf den Körper. Für das Hochfrequenzfeld sind zudem aus Sicherheitsgründen Grenzwerte definiert worden, die eine starke Erwärmung des Patienten ausschließen.
Um Schäden am Gehör des Patienten zu vermeiden, ist das Tragen eines Gehörschutzes Pflicht. Zwar werden die Klopf- und Brummgeräusche, die beim Schalten der Gradientenspulen entstehen, weitestgehend abgefangen, jedoch stellen sie eine Geräuschbelastung für den Patienten dar.12 In einigen Fällen ist es je nach Vorlieben des Patienten möglich, beruhigende Musik über Kopfhörer abzuspielen.
Während der Untersuchung erhalten Patienten aus Sicherheitsgründen eine Notfallklingel, um das medizinische Personal im Bedarfsfall auf sich aufmerksam zu machen. Insbesondere bei Patienten mit Angst vor engen Räumen kann diese Klingel zur Entspannung und zum Sicherheitsgefühl beitragen, was auch letztlich der Bildqualität der MRT-Untersuchung zuträglich ist.
Ist eine Kernspintomographie gefährlich?
Im Allgemeinen kann die MRT-Untersuchung als ungefährlich betrachtet werden, wenn die oben genannten Risiken ausgeschlossen beziehungsweise minimiert wurden. Im Gegensatz zu computertomographischen Untersuchungen kommt bei der Kernspintomographie keine ionisierende Röntgenstrahlung zum Einsatz.
Dennoch darf der MRT-Untersuchungsraum ohne vorherige Anweisung niemals betreten werden. Hierbei ist es unerheblich, ob gerade eine Messung stattfindet oder nicht, da das sogenannte statische Magnetfeld auch außerhalb von Messungen besteht. Auch der physiologische Stress, den die Untersuchung beim Patienten auslösen kann, ist nicht zu unterschätzen.
MRT-Untersuchungen trotz Platzangst?
Patientinnen und Patienten, die Angst vor der Untersuchung oder engen Räumen - umgangssprachlich als “Platzangst” bezeichnet - haben, sollten sich vor der Untersuchung bewusst machen, dass sie alleine bestimmen, wie lange die Untersuchung dauert und dass sie diese jederzeit abbrechen können. Die Ängste werden vom medizinischen Personal absolut ernst genommen und können jederzeit frei angesprochen werden, auch wenn sie aus medizinischer Sicht unbegründet sind. Viele Menschen haben Ängste vor der MRT-Untersuchung.
Es kann hilfreich sein, eine Begleitperson mit zur Untersuchung zu bringen, sich in aller Ruhe das Gerät erklären zu lassen, sich probeweise kurz auf den Untersuchungstisch zu legen und sich die verbleibende Untersuchungsdauer vom medizinischen Personal während der Untersuchung mitteilen zu lassen.
Manche Arztpraxen oder Kliniken verfügen über offene MRT-Geräte, die eine seitliche Öffnung der Röhre aufweisen und daher Patienten mit Platzangst häufig ein besseres Gefühl geben.
Bei ausgeprägter Angst ist es zudem möglich, dass dem Patienten ein Beruhigungsmittel verabreicht wird. Zuvor muss jedoch eine mögliche Wechselwirkung mit anderen Medikamenten ausgeschlossen und darauf hingewiesen werden, dass die Konzentrationsfähigkeit möglicherweise bis zum Folgetag eingeschränkt ist. Zudem sollte geklärt sein, dass der Patient nicht ohne Begleitung nach Hause geht. Zur Sicherheit werden Puls und Sauerstoffsättigung des Blutes mit einem sogenannten Pulsoxymeter überwacht.
Nach der Untersuchung sollten Patientinnen und Patienten langsam aufstehen, sich in aller Ruhe im Raum orientieren und etwas trinken. Erst wenn Schwindel und andere Beschwerden ausgeschlossen werden können, darf der Patient in Begleitung die Praxis verlassen.
MRT-Untersuchungen des Schädels
In der MRT-Diagnostik gibt es im Gegensatz zu konservativen Röntgenverfahren keine standardisierten Untersuchungen. Alle Einstellungen sind auch von dem jeweiligen Gerät abhängig und können sich sogar zwischen zwei Geräten desselben Herstellers stark unterscheiden. Die Planung der Messung erfolgt grundsätzlich in drei räumlichen Ebenen.
Eine Untersuchung des Schädels mittels Kernspintomographie kann vor allem dann hilfreich sein, wenn Schlaganfälle, Hirntumore, Kopfschmerzen, Migräne, Depressionen, Demenz, Multiple Sklerose oder Morbus Parkinson mit bildgebenden Verfahren diagnostiziert werden sollen. Weitere Erkrankungen im Kopfbereich, bei denen eine MRT eingesetzt werden kann, umfassen unter anderem Tinnitus (das Empfinden von Geräuscheindrücken, die nicht durch einen tatsächlichen Schall ausgelöst werden), Augenzittern, Schwindel, Epilepsie und Blutungen innerhalb des Schädels.
Für die Untersuchung werden Patientinnen und Patienten auf dem Rücken gelagert und gebeten, die Arme seitlich neben dem Körper abzulegen. Der Kopf wird für die Messung mit kleinen Kissen fixiert, um eine möglichst ruhige und entspannte Haltung des Patienten zu fördern und den Abstand zwischen Spule und Kopf zu gewährleisten. Zudem wird hierdurch eine Geräuschminderung erzielt und somit das Gehör des Patienten zusätzlich geschützt. Ein Gehörschutz ist dennoch unverzichtbar. Die Beine des Patienten werden zusätzlich durch eine Knierolle gestützt. Eine Notfallklingel ermöglicht es dem Patienten, während der Messung im Bedarfsfall auf sich aufmerksam zu machen.
Ist die Verabreichung eines Kontrastmittels erforderlich, so liegen zwischen Verabreichung und Messung mindestens 10 Minuten. Diese Zeit benötigt das Kontrastmittel, um zum Wirkungsort zu gelangen.
Bei Blutungen ist in einigen Fällen zur weiteren Diagnostik die Durchführung einer sogenannten MR-Angiographie erforderlich. In gesunden Geweben können Protonen ihre Energie schnell auf andere übertragen, wodurch die Magnetisierung schnell verschwindet und die Bilder dunkel erscheinen. Wenn die Protonenbewegung jedoch durch etwaige Schwellungen oder Blutungen gestört wird, geben die Protonen ein starkes Signal ab und erzeugen einen hellen Bildbereich.
Da diese als Diffusion bezeichnete Eigenschaft sehr früh Änderungen der freien Bewegung von Wassermolekülen und deren Protonen in den Räumen zwischen den Zellen zeigt, hat diese in der Infarkt- und Blutungsdiagnostik eine große Bedeutung. Man spricht dann von einer diffusionsgewichteten MRT.
Möchte man den Hirnschädel untersuchen, wählt man hierfür Messsequenzen, bei der graue und weiße Substanz des Gehirns kontrastreich dargestellt werden können.3
Perfusions-Magnetresonanztomographie
Bei der Perfusions-MRT handelt es sich um ein spezielles Kernspin-Verfahren zur Untersuchung der Perfusion, also der Durchblutung von Geweben und Organen. Informationen zum Schweregrad der Durchblutungsstörung können aus dem Verlauf der Kontrastmittelanreicherungs-Kurve im betroffenen Bereich bei einer Messung über mehrere Phasen gewonnen werden.
Während gesunde Gewebe in der Lage sind, Kontrastmittel anzureichern, sind weniger durchblutete oder bereits abgestorbene Gewebe dazu nicht in der Lage. Die bei einem Hirninfarkt entstehende Schicht zwischen abgestorbenem und gesundem Gewebe ist zwar weniger durchblutet, enthält aber noch lebensfähige Zellen und wird in der Neurologie als Penumbra bezeichnet.
Von einer irreparablen Schädigung muss ausgegangen werden, wenn die Bereiche bei der Perfusions- und der Diffusions-Messung identisch sind. Andernfalls kann das betroffene Gewebe noch gerettet werden.
Entscheidend ist die Beurteilung der Diffusion, da die Signale aufgrund der Bewegungseinschränkung der Moleküle durch zum Beispiel Schwellungen in Form von signalreichen hellen, sogenannten hyperintensen Bereichen sichtbar werden. Ein Hirninfarkt kann somit frühzeitig diagnostiziert werden.
MR-Angiographie
Die MRT ermöglicht Untersuchungen, die mit anderen Techniken nicht möglich sind. So können mittels MR-Untersuchung sämtliche Gefäße ohne den Einsatz von Kontrastmitteln dargestellt werden. Diese Methode bezeichnet man als MR-Angiographie. Es gibt prinzipiell zwei Möglichkeiten, Gefäße mittels MR-Angiographie darzustellen: (1) die Inflow-Angiographie, die auch als “time-of-flight”-Angiographie oder kurz TOF bezeichnet wird und die (2) Phasenkontrast-Angiographie, kurz PC.
Bei der “Time-of-Flight”- beziehungsweise Inflow-Methode verlieren ruhende Strukturen an Kontrast und verblassen, bewegte Strukturen hingegen erscheinen hell. Es handelt sich um eine Standarduntersuchungs-Technik der Arterien im Schädel ohne Kontrastmittel, bei der die Laufzeit des Blutes berücksichtigt wird.4 Die Signalstärke nimmt mit steigender Fließgeschwindigkeit bis zu einem bestimmten Punkt zu und aufgrund physikalischer Besonderheiten bei der Messung wieder ab. Daher ist eine Interpretation bei dieser Methode schwierig und die quantitative Bestimmung der Blutflussgeschwindigkeit nur bedingt möglich. Dennoch können Gefäße hiermit sehr gut dargestellt werden und aus den gewonnenen Daten der vollständige Gefäßbaum dreidimensional berechnet werden.
Diese auch als Inflow-Angiographie bezeichnete Methode hat den Nachteil, dass mehrere in einer Schicht liegende Blutgefäße nur schwache Signale abgeben, langsam fließendes Blut auf dem Bild nicht sichtbar ist und frische Blutgerinnsel auf dem Bild hell erscheinen können, sodass sie sich nicht vom restlichen Blut unterscheiden lassen.
Bei der Phasenkontrast-Angiographie sind die Untersuchungszeiten vergleichsweise lang und, um die Gefäße richtig darstellen zu können, ist eine exakte Einstellung der Geschwindigkeit erforderlich. Bei dieser Methode werden Bilder der Geschwindigkeitskomponente in Richtung des Gradientenfeldes bestimmt, indem man sich die bei der Messung entstehenden Phasenverschiebungen zunutze macht. Hierbei können Gefäße dargestellt werden, jedoch die Flussgeschwindigkeit innerhalb der Gefäße nicht quantitativ bestimmt werden.
Durch den Einsatz von Kontrastmitteln kann die Bildqualität der angiographischen Untersuchung um ein Vielfaches verbessert werden.
Durch Verwendung extrem schneller Pulssequenzen ist sogar die Abbildung des schlagenden Herzens mittels Magnetresonanz möglich geworden - bei der Darstellung der Herzkranzgefäße, die man auch als Koronargefäße bezeichnet, ist jedoch immer noch die Röntgen-Koronar-Angiographie die Methode der Wahl.
Funktionelle MR-Tomographie (fMRT)
Eine weitere Methode, die besonders für die Untersuchung des Gehirns von großer Bedeutung ist, wird als funktionelle Magnetresonanztomographie, kurz fMRT, bezeichnet.
Mit der fMRT können Veränderungen der Hirndurchblutung untersucht werden. Diese Technik ist allerdings relativ zeitaufwändig und die Signalausbeute gering, daher ist der klinische Einsatz begrenzt. Durch Optimierung der Methoden und eingesetzten Feldstärken können jedoch auch höhere kognitive Funktionen erfasst werden.
Hierbei macht man sich die magnetischen Eigenschaften des Hämoglobins zunutze, um vor allem funktionelle Aspekte des Gehirns darzustellen. Beim Hämoglobin handelt es sich um den eisenhaltigen roten Blutfarbstoff, der für den Transport von Sauerstoff über das Blut verantwortlich ist. Die sauerstoffarme Form, das sogenannte Desoxyhämoglobin, hat im Gegensatz zur sauerstoffreichen Form, dem Oxyhämoglobin, paramagnetische Eigenschaften. Aufgrund dieser Eigenschaften weisen Bereiche mit einem hohen Anteil des sauerstoffarmen Desoxyhämoglobins beim Einsatz bestimmter Pulssequenzen eine Abnahme des MR-Signals auf. Bereiche mit hoher lokaler Aktivität zeigen hingegen eine Zunahme in der Signalstärke, weil diese sehr schnell mit frischem, sauerstoffreichem Oxyhämoglobin versorgt werden.
Durch periodisches Ein- und Ausschalten eines Stimulus kann die natürlicherweise sehr geringe Signalstärken-Zunahme verstärkt werden, um das Signal-zu-Rauschen-Verhältnis zu optimieren. Im Prinzip kann man so eine Perfusionsmessung mit körpereigenem “Kontrastmittel” durchführen, durch die eine Abbildung aller sensorischen und motorischen Zentren des Gehirns ermöglicht wird. Diese wird als BOLD-Imaging bezeichnet. Die Abkürzung BOLD steht hierbei für die englische Bezeichnung “Blood Oxygenation Level Dependent Contrast”, also einen Kontrast, der vom Sauerstoffgehalt des Blutes abhängt. Idealerweise setzt man diese MRT-Variante ergänzend zu anderen funktionellen Bildgebungsverfahren ein.
Einsatz von Kontrastmitteln bei der Kernspintomographie
Bereits der Einsatz unterschiedlicher Pulssequenzen kann die Kontraste im MR-Bild enorm verändern. Durch den gezielten Einsatz von Kontrastmitteln kann je nach diagnostischer Fragestellung eine weitere Optimierung der Bilddarstellung vorgenommen werden.
Die Dichte an Protonen im Gewebe kann nur schwer verändert werden. Jedes bei der MRT genutzte Kontrastmittel setzt daher bei einer Veränderung der Pulssequenzen an. Wird über die Vene ein Kontrastmittel verabreicht, kommt es zu einer Verstärkung bestimmter Wechselwirkungen und somit zur Verkürzung der Pulssequenzen.
Durch die verabreichten Kontrastmittel kann es zu allergischen Reaktionen kommen. Häufige Nebenwirkungen umfassen Übelkeit und Erbrechen sowie Juckreiz. In einigen Fällen können Schleimhautschwellungen, Quaddelbildungen und Atembeschwerden auftreten. Auch starke Nebenwirkungen, wie ein anaphylaktischer Schock, können in seltenen Fällen als Reaktion auf das Kontrastmittel auftreten.
Zwar treten allergische Reaktionen bei diesen Mitteln in der Regel seltener auf, als zum Beispiel bei den in der Computertomographie eingesetzten jodhaltigen Kontrastmitteln, dennoch ist das medizinische Personal hervorragend mit entsprechenden Notfallmedikamenten auf solche Fälle vorbereitet.
Als Kontrastmittel für die MRT eignen sich sogenannte paramagnetische Substanzen, wie zum Beispiel Gadolinium, die im Magnetfeld magnetische Eigenschaften besitzen. Viele Gadolinium-Verbindungen sind hochgiftig, das gilt jedoch natürlich nicht für die verwendeten Kontrastmittel. Wird nach Verabreichung der nicht-giftigen Gadoliniumverbindung eine bestimmte Art von MR-Aufnahme gemacht, erscheint das mit dem Kontrastmittel angereicherte Gewebe durch das erhöhte Signal hell im Vergleich zum umliegenden Gewebe.
Nach der Anwendung Gadolinium-haltiger Kontrastmittel kann es einer umfassenden Bewertung durch die Europäische Arzneimittelagentur EMA im Januar 2018 zufolge zu einer Ablagerung geringer Mengen Gadolinium im Gehirn kommen - bislang gibt es jedoch keine Hinweise auf eine Schädigung der Patienten durch diese Ablagerung. Derartige Ablagerungen scheinen sich zu bilden, wenn Gadolinium-haltige Kontrastmittel über die Vene für MRT-Untersuchungen verabreicht werden.
Trotz der bisher vermeintlichen Unbedenklichkeit soll der Einsatz Gadolinium-haltiger Kontrastmittel nur für diagnostische Zwecke erfolgen, wenn MRT-Untersuchungen ohne diese nicht die nötigen Informationen liefern. Zudem erfolgt grundsätzlich der Einsatz der niedrigsten Dosis, die ausreichende Informationen für die Diagnose liefert.13
Andere Arten von Kontrastmitteln führen zu einem reduzierten Signal, wenn sie in einem bestimmten Aufnahmemodus erstellt werden. Auch die beiden ionischen Kontrastmittel Magnevist und Gadovist sowie das nicht-ionische Kontrastmittel Dotarem werden in der Praxis häufig verabreicht.
In jedem Fall ist es hilfreich, die Aufnahmen nach Kontrastmittelgabe mit Aufnahmen zu vergleichen, die vor der Verabreichung des Kontrastmittels in gleicher Einstellung durchgeführt wurden.3
Die Pharmaindustrie ist an der Entwicklung immer neuer MR-Kontrastmittel für spezielle Fragestellungen interessiert. Vor allem sollen Verbindungen gefunden werden, die im Stoffwechsel involviert sind und mit deren Hilfe funktionsdiagnostische Aufnahmen - ähnlich der Positronen-Emissions-Tomographie, kurz PET - erfolgen können.
Bei einem völlig neuartigen Ansatz soll der Weg des Kontrastmittels durch den Körper verfolgt werden, indem man es an eine bestimmte Art von Antikörpern koppelt.
Die Kernspintomographie in der Schlaganfall-Diagnostik
Akute ischämische Schlaganfälle weisen in bildgebenden Verfahren einige Veränderungen auf, die durch die drei Stadien entstehen, die sie durchlaufen: (1) die Ödemphase, (2) die Abräumphase und (3) die Narbenphase.
Bei der ersten Phase, der Ödemphase, kommt es sofort nach dem akuten Auftreten eines Gefäßverschlusses im Gehirn durch ein Blutgerinnsel - dem Thrombus - oder durch Stücke von Fettablagerungen im Rahmen der Arteriosklerose zu einer zellschädigenden Schwellung des Gehirns. Diese wird als zytotoxisches Hirnödem bezeichnet. Innerhalb von sechs Stunden entwickelt sich ein weiteres Ödem im Gewebe-Zwischenraum. Nach wenigen Tagen bildet sich dann ein deutlich raumforderndes Ödem. Die gesamte Phase umfasst etwa eine Woche. Die erste Form des Hirnödems kann im MRT bereits nachgewiesen werden, da der Infarktkern sich mittels diffusionsgewichteter MR-Bildgebung schon nach wenigen Minuten darstellen lässt.1
Die CT zeigt im Vergleich dazu hingegen erst nach 6-10 Stunden positive Befunde. Das raumfordernde Ödem ist mittels CT und MRT gleichermaßen nach etwa 2-3 Tagen nachweisbar. Die MRT kann darüber hinaus eine Störung der Blut-Hirn-Schranke unter Einsatz von Kontrastmitteln meist nach etwa drei Tagen nachweisen, da sich das Kontrastmittel in oder um den Infarkt anreichert. Mittels CT ist dieser Nachweis erst nach etwa sieben Tagen möglich.
Im Verlauf der sogenannten Abräumphase bildet sich das Ödem zurück und das abgestorbene Gewebe wird abgebaut. In dieser etwa zwei- bis fünfwöchigen Phase wird die Störung der Blut-Hirn-Schranke mittels kontrastmittelverstärkter MRT und CT sichtbar. Die Kernspintomographie ist hierbei der CT als Nachweismethode überlegen und zeigt diffuse, kleinfleckige Einblutungen.
Die dritte und letzte Phase akuter ischämischer Schlaganfälle wird als Narbenphase bezeichnet, weil es etwa in der 6. Woche nach Auftreten kleiner Hirninfarkte zur Ausbildung einer Narbe kommt. Bei großen Hirninfarkten entsteht im Vergleich dazu ein flüssigkeitsgefüllter Gewebedefekt. Dieser kann sowohl im CT als auch im MRT deutlich dargestellt werden.
Soll der Gefäßverschluss mechanisch mittels Thrombektomie oder medikamentös mittels Thrombolyse wiedereröffnet werden, kann noch eine anschließende MR-Angiographie oder CT-Angiographie erfolgen. Als rein diagnostische Maßnahme werden diese jedoch bei akuten ischämischen Schlaganfällen nicht eingesetzt.
Die Abgrenzung des akuten ischämischen Schlaganfalls gegenüber der Hirnblutung, dem sogenannten hämorrhagischen Schlaganfall, kann mittels nativer MRT oder CT erfolgen. Bei Verschluss einer basalen größeren Hirnarterie kann die Diagnose zuverlässig mittels MR-Angiographie gestellt werden. Die Blutgefäße können hierbei ohne Kontrastmittel abgebildet werden. Soll der Infarktkern automatisiert dargestellt werden, ist die Untersuchung mittels diffusionsgewichteter Magnetresonanz-Methode einfacher als mittels CT, da gesundes und von Infarkt betroffenes Gewebe größere Signalunterschiede liefern. Gleiches gilt, wenn es darum geht, die vollständige Infarkt-Ausdehnung zu erfassen.13
Diffusionsgewichtete Bildgebung ermöglicht die Quantifizierung der Bewegung von Wassermolekülen unter anderem im Gehirn und hat die Magnetresonanztomographie revolutioniert. Die Diffusions-MRT ist heute Bildgebungsmethode der Wahl für Schlaganfall-Patientinnen und -Patienten. Die verschiedenen Gewebe des menschlichen Körpers haben eine charakteristische Architektur und somit auch charakteristische Diffusionseigenschaften.15 Diffusion beschreibt einen physikalischen Vorgang, bei dem die zufällige Bewegung von Molekülen für den Ausgleich von Konzentrationsunterschieden sorgt.
Im Gehirn ist die Bewegung der Moleküle durch die Mikrostruktur der grauen und weißen Hirnsubstanz eingeschränkt. Ohne Zwang würde sich ein Wassermolekül zufällig und gleichmäßig in alle Richtungen bewegen. In geordneten Umgebungen, wie zum Beispiel der weißen Hirnsubstanz, erfolgt die Bewegung gerichtet in elliptischen Bahnen.16 Bei einem akuten Hirninfarkt ist der intrazelluläre Wasseranteil des betroffenen Gewebes erhöht und somit die Diffusionsbewegung eingeschränkt. Die diffusionsgewichtete Bildgebung liefert qualitative und quantitative Informationen über die Diffusionseigenschaften. Gewebe mit eingeschränkter Diffusion erscheinen hell.
Die diffusionsgewichtete (DWI) Untersuchung ist der wichtigste Test in der Diagnostik ischämischer Schlaganfälle und wurde erstmals in den frühen 1990ern zu diesem Zweck eingesetzt.16 In einigen Fällen kann es jedoch sein, dass die Untersuchung negativ - also ohne Befund - ausfällt, obwohl ein ischämischer Schlaganfall mit neurologischen Ausfällen vorliegt. Chinesische Wissenschaftler haben kürzlich jedoch einige Biomarker des menschlichen Immunstoffwechsels identifiziert, mit deren Hilfe auch bei DWI-negativen Befunden der Nachweis eines ischämischen Schlaganfalls möglich sein soll, da das Immunsystem nach einer Ischämie aktiviert wird.17 Biomarker sind charakteristische biologische Eigenschaften, mit deren Hilfe man gesunde von krankhaften Prozessen im Körper unterscheiden kann.
Modernes Schlaganfall-Management setzt die Diffusions-MRT in Kombination mit einer Perfusions-MRT und MR-Angiographie ein.15
Die Möglichkeiten zur Darstellung ischämischer Schlaganfälle mittels Magnetresonanztomographie werden stets weiterentwickelt und erforscht. Aktuelle Studien, wie eine prospektive Studie von Forschenden der Universitätsmedizin Mainz, untersuchen vor allem die Möglichkeiten, die sich durch den Einsatz künstlicher Intelligenz bei MRT-Untersuchungen eröffnen. Durch Verwendung bestimmter Algorithmen bei der Bildrekonstruktion ist es demnach möglich, eine höhere Bildqualität und eine deutlich schnellere Bildgebung zu erzielen. Dadurch wird die Notfalldiagnostik bei Verdacht auf Vorliegen eines Schlaganfalls revolutioniert. Ischämische Schlaganfälle können deutlich schneller behandelt und auch leichte Schlaganfälle mit höherer Wahrscheinlichkeit nachgewiesen werden.18
Durch den Einsatz künstlicher Intelligenz, kurz als KI bezeichnet, könnte es künftig sogar möglich sein, Schlaganfälle mit weitaus kostengünstigeren Geräten zu nachzuweisen als mit den modernsten Hochleistungs-MRTs. Dies legen die Forschungsergebnisse einer Gruppe chinesischer Forscher nahe, die die Möglichkeiten der Bilddarstellung mit Geräten geringerer Leistung untersucht haben. Gehirnstrukturen und -gewebe konnten demnach klar voneinander unterschieden und die Bildqualität durch die sogenannte “Deep Learning” Methode, einer KI-Technik, deutlich verbessert werden. Rauschen und Bildfehler wurden durch den KI-Einsatz wirksam unterdrückt und die räumliche Auflösung der Bilder erhöht.19
Völlig neuartige Ansätze liefert auch das Massachusetts Institute of Technology, kurz MIT: MIT-Wissenschaftlern ist es gelungen, Licht unter Einsatz von Magnetresonanz-Bildgebung in tiefliegenden Gehirnstrukturen nachzuweisen. Hierdurch könnten detaillierte Studien der Gehirnzellentwicklung und -kommunikation möglich werden, die auch in der Schlaganfall-Diagnostik wertvolle Informationen liefern würden. Während bislang der Einsatz leuchtender Proteine sehr gut in einigen Zellen und Geweben funktionierte, war es durch die sehr starke Streuung des Lichts schwierig, diese Biolumineszenz-Technik im Inneren des Gehirns erfolgreich anzuwenden. Die MIT-Wissenschaftler haben es geschafft, dass die Blutgefäße im Gehirn durch genetische Veränderungen ein Protein herstellen, das in Anwesenheit von Licht zur Blutgefäßerweiterung führt, der sogenannten Vasodilatation. Diese kann kernspintomographisch beobachtet und die Lichtquelle exakt lokalisiert werden.20
Ist die MRT der CT in der Schlaganfall-Diagnostik überlegen?
Diese Frage lässt sich nicht pauschal beantworten, jedoch gibt es Kriterien, die den Einsatz der MRT als Methode der Wahl bei der Schlaganfall-Diagnostik stützen. In der Notfallsituation wird allerdings wegen der kürzeren Untersuchungszeit und der sicheren Unterscheidung zwischen einem Hirninfarkt durch Blutmangel und einer Hirnblutung die kraniale Computertomographie bevorzugt eingesetzt.
Vor allem beim Nachweis eines frischen Hirninfarktes bietet die Kernspintomographie entscheidende Vorteile, da schon kurze Zeit nach dem ischämischen Schlaganfall mittels MRT eine Zunahme der Signalintensität bei T2-gewichteter Pulssequenz dokumentiert werden kann. Nutzt man diffusions- und perfusionsgewichtete Aufnahmen, ist bereits innerhalb weniger Minuten der Hirninfarkt nachweisbar. Kleine punktförmige Blutungen - sogenannte Petechien - im Infarktbereich können ebenfalls durch die MRT besser dargestellt werden, als durch entsprechende computertomographische Methoden.
Dennoch wird die MRT zur Schlaganfall-Diagnostik meist nur zur Beantwortung spezieller Fragestellungen oder bei Schlaganfall-Studien eingesetzt, da die Untersuchung unter anderem eine starke Mitwirkung des Patienten erfordert, um Messfehler durch ungewollte Bewegung zu vermeiden. Vor allem aufgrund der Untersuchungsdauer kann dies in einigen Fällen jedoch erschwert werden.
Vor- und Nachteile der Magnetresonanz-Tomographie
Ein großes Potenzial besitzt die MRT dadurch, dass man durch unterschiedliche Einstellung der MRT-Parameter völlig verschiedene Bilder von ein und demselben Untersuchungsbereich erzeugen kann.
Durch Anpassung der Pulssequenz hat man viele Möglichkeiten der Bildoptimierung, wodurch erkrankte Gewebe optimal dargestellt werden können. Basierend auf Erfahrungswerten wurden bereits für zahlreiche Erkrankungen die optimalen Pulssequenzen ermittelt, sodass ohne langes Optimieren direkt die passenden Aufnahmeparameter eingestellt werden können.
Einen entscheidenden Vorteil gegenüber der computertomographischen Untersuchung bietet die MRT bei der Erfassung von Strukturen der Hirnbasis und des Spinalkanals, da Weichteile mittels MR-Tomographie kontrastreicher dargestellt werden und keine Störungen durch Knochenartefakte auftreten. Insbesondere für krankhafte Prozesse im Nervensystem hat sich die MRT als hochsensitive Methode mit hervorragender Kontrastauflösung erwiesen. Auch bei der Erfassung von Gefäßfehlbildungen im Gehirn, sogenannten Aneurysmen, ist die Kernspintomographie der Computertomographie überlegen.
Sollen Tumoren dargestellt werden, ist die MRT gegenüber der CT das Verfahren der Wahl.3
Grundsätzlich sind Bewegungen des Körpers die größte Fehlerquelle bei MRT-Untersuchungen, die grundsätzlich zeitintensiver sind als beispielsweise CT-Untersuchungen. Patientinnen und Patienten müssen also vergleichsweise lange ruhig liegen, um hochqualitative, fehlerfreie Bilddaten zu erhalten. Je nach Lage des Patienten ist das nur sehr schwer umzusetzen.
Auch die Kosten einer Kernspintomographie-Untersuchung des Schädels liegen deutlich höher als die einer Computertomographie-Untersuchung.
Letztlich entscheiden immer die medizinische Fragestellung und die Krankenvorgeschichte des Patienten darüber, welches Bildgebungsverfahren sich zur Diagnosestellung besser eignet.
Was kostet eine Untersuchung mittels Kernspintomographie?
Die Kosten für eine Kernspintomographie variieren je nach Untersuchungsbereich und liegen bei privat Versicherten zwischen 140 und 2.000 Euro, bei gesetzlich Versicherten zwischen 125 und 375 Euro. Diese Unterschiede resultieren daraus, dass die Kosten bei den gesetzlichen Krankenkassen fest definiert sind, während die Kosten bei den privaten Krankenversicherungen von der sogenannten Gebührenordnung für Ärzte und weiteren Faktoren abhängen. Eine wichtige Information für gesetzlich versicherte Patientinnen und Patienten ist, dass kernspintomographische Untersuchungen des Herzens und Ganzkörper-Scans keine Kassenleistung sind und somit selbst von den Patienten gezahlt werden müssen.
Bei gesetzlich versicherten Patienten betragen die Kosten für eine MRT-Untersuchung des Kopfes beispielsweise rund 125 Euro. Die Kosten bei Privatpatienten belaufen sich auf etwa 255 bis 460 Euro. Im Vergleich dazu fallen die Kosten bei einer CT-Untersuchung des Schädels mit rund 167 Euro geringer aus. Diese werden unabhängig von der Versicherungsart des Patienten nach der sogenannten Gebührenordnung für Ärzte mit den Krankenkassen abgerechnet.21
Wissenswertes rund um die Kernspintomographie
Die MRT ist ein schmerzfreies, sehr effizientes bildgebendes Verfahren, mit dem der menschliche Körper oder einzelne Körperteile hochauflösend dreidimensional dargestellt werden können. Genau aus diesem Grund erfreut sich diese Technik zunehmender Beliebtheit, was sich in einem deutlichen Aufwärtstrend in den durchgeführten Untersuchungen widerspiegelt. Allein in Deutschland werden 97 Untersuchungen pro 1000 Einwohner jährlich durchgeführt - das sind ganze 2 Millionen MRT-Untersuchungen insgesamt. Internationale Vergleiche zeigen, dass Deutschland Spitzenreiter ist, wenn es um den Einsatz der Kernspintomographie zur Diagnosestellung geht. Besonders, wenn es um die Untersuchung von Erkrankungen und Verletzungen im Kopfbereich geht, liegen die beiden bildgebenden Verfahren MRT und CT weit vorne mit 4,67 Millionen Untersuchungen pro Jahr.10
Die MRT-Technik wird kontinuierlich weiterentwickelt und verfeinert. Unter anderem wurden neue Sensor-Prototypen entwickelt, die mittels Laserlicht und Gas in der Lage sind, Fehler in MRT-Scans zu erkennen. Die bisherigen elektrischen Sensoren können dies nicht. Durch die neue Art der Fehlererkennung könnten MRT-Scans künftig möglicherweise schneller, kostengünstiger und zugleich besser werden.22
Im Rahmen des Iseult-Projekts wurde der wohl leistungsstärkste MR-Tomograph entwickelt, der mit einer weltweit unübertroffenen Magnetfeldstärke von 11,7 Tesla ausgestattet ist. Mit diesem MRT-Gerät soll es möglich werden, das Gehirn in noch nie dagewesener Auflösung zu untersuchen und die exzellente Darstellung der anatomischen Strukturen, Gehirnverbindungen und -aktivitäten zu ermöglichen. Die bislang beeindruckendsten anatomischen Bilder des Gehirns konnten in nur vier Minuten mit dem Iseult-MRT-Gerät erzeugt werden. Mit herkömmlichen in Krankenhäusern aktuell eingesetzten Geräten würde es im Vergleich dazu Stunden dauern, um die gleiche Bildqualität zu erhalten - was ganz nebenbei technisch und logistisch kaum möglich wäre.23
Bei diesen neuartigen Entwicklungen handelt es sich um Technik, die noch nicht den Weg in die alltägliche Praxis gefunden hat. Die Neuanschaffung und Installation eines Magnetresonanztomographen der aktuellen Generation, wie er aktuell in Kliniken eingesetzt wird, ist enorm kostenintensiv. Laut dem Medizintechnik-Onlineportal Medizinio liegen die Kosten zwischen 750.000 und 3.500.000 Euro. Bei gebrauchten Geräten variieren die Kosten je nachdem, ob es sich um ein geschlossenes oder offenes MRT handelt. Die Anschaffungskosten für offene MR-Tomographen liegen mit 160.000 bis 1.500.000 Euro weitaus höher, als die für geschlossene Geräte mit 30.000 bis 100.000 Euro. Neben Verbesserungen der Bildqualität bleibt somit die Entwicklung kostengünstigerer Varianten ein Hauptziel der weiteren Forschung.
Aufbau und Funktionsweise der MRT
Physikalisches Prinzip der MRT
Die Kernspintomographie ist in der Lage, ohne den Einsatz von Röntgenstrahlung Schnittbilder des menschlichen Körpers in frei wählbaren Raumebenen zu erzeugen. Dadurch grenzt sie sich von einem weiteren häufig genutzten Verfahren zur Erzeugung von Schnittbildern ab: der Computertomographie, kurz CT. Die Kernspintomographie nutzt Eigenschaften der Atome, die natürlicherweise im menschlichen Körper vorkommen.
Im menschlichen Körper vorhandene Wasserstoffprotonen eignen sich hervorragend zur Erzeugung von Signalen, die mittels MRT gemessen und dargestellt werden können. Wasser (H2O) ist das mit bis zu 70 Prozent im Körper am häufigsten vorkommende Molekül, wodurch eine Vielzahl an Wasserstoffatomen und ihre im Kern vorliegenden positiv geladenen Teilchen, die Protonen, für die Untersuchung zur Verfügung stehen.
Die MRT nutzt hierbei eine Eigenschaft der Protonen, die als Kernspin bezeichnet wird und dafür sorgt, dass jedes Proton einen Eigendrehimpuls besitzt. Hierdurch entstehen im Körper ungerichtete Magnetfelder, die sich bei der Erzeugung eines starken äußeren Magnetfeldes parallel oder antiparallel entlang der Kraft des äußeren Magnetfeldes ausrichten.
Die Bewegung, mit der sich die Atomkerne der Wasserstoffatome um die Längsachse des Magnetfeldes drehen, wird als Präzession bezeichnet. Ist das äußere Magnetfeld stark genug, kann es die Geschwindigkeit (Frequenz) vorgeben, mit der die Ladung der Protonen rotiert. Man spricht dann von Präzessions- oder Larmorfrequenz.
Dadurch wird das Phänomen der sogenannten Resonanz ermöglicht, bei der Energie auf die Protonen übertragen wird, was man als Anregung bezeichnet. Hierzu wird ein Hochfrequenzimpuls eingesetzt, der nach dessen Abschaltung bewirkt, dass die Protonen die aufgenommene Energie wieder in Form eines magnetischen Impulses abgeben. Dieser Impuls ist messbar, wodurch mittels MRT Daten erzeugt werden, die anschließend in ein Bild umgerechnet werden können.
Die Protonen kehren nach der Anregung in ihren ursprünglichen Zustand zurück, was als Relaxation bezeichnet wird. Dieser Vorgang kann mathematisch durch Zeitkonstanten beschrieben werden, die spezifisch für das jeweilige Gewebe sind.
Die entsprechenden Zeitkonstanten heißen T1 beziehungsweise Spin-Gitter-Relaxationszeit und T2, die auch als Spin-Spin-Relaxationszeit bezeichnet wird. Beide Zeitkonstanten bewegen sich im Millisekunden-Bereich, wobei T2 deutlich kürzer ausfällt als T1.
Um das Rauschen, also Störfaktoren bei der Messung zu eliminieren, ist eine mehrfache Anregung - eine sogenannte Pulssequenz - erforderlich. Hierdurch entstehen zwei weitere Kenngrößen der MRT-Messung: (1) die Repetitionszeit TR und (2) die Echozeit TE.
Als Repetitionszeit wird die Zeit zwischen zwei Anregungen bezeichnet. Die Echozeit stellt hingegen die Zeit zwischen der Anregung und dem Signal dar. Die gemessenen Daten werden gemittelt.
Während sich eine Pulssequenz besonders gut für anatomische Darstellungen eignet, werden bei Verwendung einer anderen Pulssequenz wiederum pathologische Veränderungen sehr gut sichtbar. Die Wahl der Pulssequenz richtet sich also nach der jeweiligen Fragestellung. Die entsprechenden Bilder unterscheiden sich vor allem darin, welche Bereiche signalintensiv - also hell - dargestellt werden und welche eher signalarm als dunkle Bereiche erscheinen.3
Um die empfangenen Signale in ein auswertbares Bild umzuwandeln, werden verschiedene Pulssequenzen verwendet, die alle den gleichen Grundaufbau besitzen. Die Wahl der Sequenz-Gewichtung bestimmt den Bildkontrast.
Abhängig von Gewebeparametern wie den Zeitkonstanten T1 und T2 sowie den Sequenzparametern TR und TE und dem Sequenztyp kann Einfluss auf den Bildkontrast genommen werden. Dadurch wird es möglich, unterschiedliche medizinische Fragestellungen optimal zu beantworten. Man unterscheidet 3 Formen der Sequenz-Gewichtung:
- Ist die Sequenz T1-gewichtet, liegen kurze Repetitionszeiten und Echozeiten vor. Bei hellen, sogenannten hyperintensen Bereichen wie zum Beispiel der weißen Hirnsubstanz und Fett handelt es sich um Gewebe mit einer kurzen T1. Gewebe wie die graue Hirnsubstanz oder Muskelgewebe werden dunkel, also hypointens dargestellt. Es handelt sich um Gewebe mit langer T1.
- Längere Repetitions- und Echozeiten sind charakteristisch für T2-gewichtete Sequenzen. Wasser erscheint bei dieser Gewichtung zum Beispiel hell, da es sich um ein Gewebe mit einer langen T2 handelt. Muskelgewebe erscheint als Gewebe mit kurzer T2 dunkel. Bei dieser Gewichtung sind Gehirnflüssigkeit (Liquor), Schwellungen im Gehirn - sogenannte Ödeme - und wassergefüllte Zysten als helle Bereiche auf dem MRT-Bild erkennbar.
- Die dritte Form der Sequenzgewichtung wird als PD-Gewichtung bezeichnet. PD steht für "Protonendichte". Hier liegt eine lange Repetitionszeit, aber eine kurze Echozeit vor. T1 und T2 haben hier einen vernachlässigbaren Einfluss. Wasser und Bindegewebe besitzen eine hohe PD und erscheinen daher hell, Knochen und Luft als Gewebe mit geringer PD erscheinen dunkel.
Wie ist ein MR-Tomograph aufgebaut?
Im Gegensatz zum Computertomographen enthält ein Magnetresonanztomograph - abgesehen vom Untersuchungstisch - keine bewegten Teile.
Der MR-Magnet
Eine der wichtigsten Komponenten des MR-Tomographen ist der Magnet, der den größten und schwersten Teil ausmacht und das statische Hauptmagnetfeld erzeugt. Je stärker das Magnetfeld ist, desto besser ist auch das Signal-zu-Rauschen-Verhältnis, desto länger ist jedoch auch die Aufnahmezeit.
In Abhängigkeit von der Magnetfeldstärke werden vier verschiedene Gruppen von MRT-Geräten unterschieden: (1) niedrig, (2) mittel, (3) hoch und (4) ultrahoch. Diese unterscheiden sich in der Art des Magneten, der verwendet wird.
Sogenannte Permanentmagneten sind für Routineuntersuchungen häufig nicht geeignet, weil sie nur sehr schwache Magnetfelder erzeugen. Elektromagneten sind zwar mit mittlerer Magnetfeldstärke besser geeignet, haben aber den Nachteil, dass sie durch hohen Stromverbrauch vergleichsweise kostenintensiv sind. Am häufigsten werden daher supraleitende Magnete in modernen Systemen verwendet, die sich ein physikalisches Prinzip zunutze machen, bei dem der elektrische Widerstand bei Temperaturen um -273,15 °C, dem absoluten Nullpunkt der thermodynamischen Temperaturskala, extrem abnimmt. Man verwendet hierbei in den meisten Fällen flüssiges Helium, um solch extrem niedrige Temperaturen zu erreichen.7
In der Praxis haben sich Magnete mit mittleren Feldstärken für die meisten Messungen durchgesetzt, da diese das beste Preis-Leistungs-Verhältnis haben. Der Magnet befindet sich in einem Magnettunnel, dem ringförmigen Teil des MRT-Gerätes, der umgangssprachlich auch als “Röhre” bezeichnet wird.
Die Gradientenspulen
Die Gradientenspulen sind fest verbaute Magnetspulen und befinden sich in der Röhrenwand des MRT-Gerätes. Sie dienen der Erzeugung eines Feldgradienten, indem Strom durch die Windungen der Spulen fließt. Die Gradientenspulen sind in die 3 räumlichen Hauptrichtungen x, y und z ausgerichtet und ihre Einschaltung erfolgt einzeln oder in Kombination.
Sind die erzeugten Magnetfelder instabil, kommt es zu Bildverzerrungen. Die Vibration in den Gradientenspulen ist für das typische “hämmernde” oder “klopfende” Geräusch bei MRT-Untersuchungen verantwortlich.
Die Sende- und Empfangsspulen
Mit der sogenannten Sende- und Empfangsspule wird quer zur Längsrichtung des MRT-Magneten ein rotierendes Magnetfeld aufgebaut und das erzeugte Resonanzsignal registriert.
Wie auch die Gradientenspule liegt diese in der Röhrendwand des MR-Tomographen und ist für die Erzeugung des pulsierenden Magnetfeldes und der Radiowellen zuständig. Die HF-Sende- und Empfangsspulen können entweder als einzelne Spulen verbaut oder zu einer gemeinsamen Spule kombiniert sein. Die Hochfrequenzen (HF) der Sendespule, die bei der Untersuchung zum Einsatz kommen, sind für den Menschen ungefährlich.
Die Shim-Spulen
Aufgabe der sogenannten Shim-Spule ist es, etwaige Unregelmäßigkeiten des Magnetfeldes zu korrigieren und auszugleichen. Der Begriff stammt ursprünglich aus der englischen Sprache und bedeutet so viel wie “Unterlegscheibe” oder "Keil".
Der Hochfrequenz-Generator und der Empfangsteil
Zur Erzeugung des zu sendenden Signals verwendet man meistens sogenannte Synthesizer.
Das Computersystem der MR-Anlage mit Bedienkonsole
Das Computersystem der MR-Anlage befindet sich meist in einem separaten, vor magnetischer Strahlung abgeschirmten Raum und dient der Steuerung und Überwachung des MR-Tomographen, der Berechnung der Bilder aus den gemessenen Signalen und der Datenspeicherung. Es verfügt über einen Hochleistungsrechner mit entsprechenden Bildbearbeitungsprogrammen, mit deren Hilfe im Anschluss an die Untersuchung ein optimaler Bildbefund erstellt werden kann.
Praxis-Tipps
- Machen Sie sich mit dem MRT-Gerät vertraut und sprechen Sie das medizinische Fachpersonal auf mögliche Bedenken und Ängste an.
- Tragen Sie zur MRT-Untersuchung möglichst bequeme Kleidung ohne Reißverschlüsse oder metallische Knöpfe. Sie sollten sich möglichst wohl fühlen.
- Weisen Sie das medizinische Fachpersonal auf Erfahrungen hin, die Sie in der Vergangenheit bei MRT-Untersuchungen gemacht haben. Haben Sie möglicherweise schon einmal ein Kontrastmittel verabreicht bekommen, das Sie nicht gut vertragen haben? Oder mussten Sie eine MRT-Untersuchung abbrechen, weil Ihre Angst davor zu groß war? Teilen Sie diese Erfahrungen gerne dem behandelnden Personal mit.
- Informieren Sie sich in aller Ruhe vor der Untersuchung über mögliche Risiken. Viele Ängste können durch gute Aufklärung im Vorfeld genommen werden.
- Setzen Sie vor der Untersuchung gegebenenfalls Entspannungstechniken ein, die Ihnen helfen, für die Dauer des MRT-Scans ruhig zu bleiben. Dies können Atemtechniken sein, aber auch andere Methoden. So können Sie dazu beitragen, die Untersuchung möglichst stressfrei für Sie zu gestalten.
- Bleiben Sie wenn möglich ruhig in der Position liegen, in der sie das medizinische Personal auf dem Untersuchungstisch gelagert hat. Bei etwas schwierigeren Haltungen oder Erkrankungen, die eine Lagerung für die Dauer der Untersuchung erschweren, werden Sie durch entsprechende Hilfsmittel, wie zum Beispiel durch Kissen und Gurte, dabei unterstützt.
- Folgen Sie zu jeder Zeit den Anweisungen des Personals. Dieses ist erfahren in der Anwendung der MRT und kann daher für Ihre Sicherheit sorgen.
Sie möchten eine schnelle Antwort? Dann fragen Sie unsere KI-Assistentin Lola.
- Untersuchungen und Diagnose des Schlaganfalls
- Computertomographie (CT) - Ablauf, Strahlung, Kosten und Praxis-Tipps
- EEG – Elektroenzephalographie - Funktionsweise, Ablauf, Risiken und Kosten
- Was ist ein Schlaganfall?
- Was sind die Symptome eines Schlaganfalls?

Bestellen Sie jetzt unseren Newsletter! Wir schicken Ihnen regelmäßig und kostenlos aktuelle Informationen rund zum Schlaganfall: Grundlagen-Informationen, Ratgeber, konkret umsetzbare Tipps und aktuelle Studien.
Die Zeit nach der Klinik ist für Angehörige oft die größte Herausforderung. Unser Online-Kurs führt Sie in 13 kompakten Modulen durch die Zeit danach. Der Kurs ist ein kostenfreies Angebot gesetzlicher Krankenkassen nach § 45 SGB XI.
Artikel aktualisiert am: - Nächste geplante Aktualisierung am:

Autoren
Dipl.-Biol. Claudia Helbig unter Mitarbeit von Prof. Dr. med. Hans Joachim von Büdingen
Claudia Helbig ist Diplom-Human- und Molekularbiologin und hat zuvor eine Ausbildung zur Arzthelferin absolviert. Als wissenschaftliche Mitarbeiterin der Medizinischen Biochemie und Molekularbiologie hat sie Medizinstudenten in Pathobiochemie-Seminaren und Praktika betreut. Nach Ihrer Arbeit in der pharmazeutischen Forschung hat sie in einem Auftragsforschungsinstitut für klinische Studien unter anderem Visiten mit Studienteilnehmern zur Erhebung von Studiendaten durchgeführt und Texte für die Website verfasst. Mit ihrem interdisziplinären Hintergrund und ihrer Leidenschaft zu schreiben möchte sie naturwissenschaftliche Inhalte fachlich fundiert, empathisch und verständlich an Interessierte vermitteln. [mehr]
Quellen
- Bildgebende Verfahren in der Medizin, 2. Auflage - Autor: Dössel, Olaf - Publikation: Springer Vieweg Verlag Berlin Heidelberg 2016 - DOI: 10.1007/978-3-642-54407-1
- Duale Reihe Radiologie, 4., vollständig überarbeitete Auflage - Autoren: Reiser, Maximilian; Kuhn, Fritz-Peter; Debus, Jürgen - Publikation: Georg Thieme Verlag Stuttgart 2017 - DOI: 10.1055/b-004-132212
- Klinische Neuroanatomie - kranielle MRT und CT, 4. Auflage (2015) - Autoren: Lanfermann, Heinrich; Raab, Peter; Kretschmann, Hans-Joachim; Weinrich, Wolfgang - Publikation: Georg Thieme Verlag Stuttgart 2015 - DOI: 10.1055/b-003-127184
- Duale Reihe Neurologie, 7., vollständig überarbeitete und erweiterte Auflage - Autoren: Masuhr, Karl F.; Masuhr, Florian; Neumann, Marianne - Publikation: Georg Thieme Verlag Stuttgart 2013 - DOI: 10.1055/b-003-106487
- Aufbau eines MRT-Gerätes (im Buch: MRT der Gelenke und der Wirbelsäule; S. 33-36) - Autor: Beyer, Hans-Konrad - Publikation: Springer Verlag Berlin - Heidelberg 2003 - DOI: 10.1007/978-3-642-55816-0_6 - Online ISBN: 978-3-642-55816-0
- Magnetresonanztomographie - MRT; Universitätsklinikum des Saarlandes und Medizinische Fakultät der Universität des Saarlandes; (abgerufen am 15.07.2024) - Autor: Prof. Dr. Lipp, Peter - URL: https://www.uniklinikum-saarland.de/de/einrichtungen/fachrichtungen/zellbiologie/seminar_zellbiologie_20192020/magnetresonanztomographie_mrt/aufbau/
- Magnetresonanztomographie für MTRA/RT; 1. Auflage 2012 - Autor: Trzebiatowski, Elisabeth - Publikation: Georg Thieme Verlag; Stuttgart - New York; 2012 - ISBN: 9783131670816
- MRT Kopf Untersuchung: Gründe, Ablauf, Dauer, Kosten; pA Medien GmbH; 2023 (abgerufen am 18.07.2024) - URL: https://www.praktischarzt.de/untersuchungen/mrt/kopf/
- Magnetresonanztomographie (Kernspintomographie; MRT); Uniklinik RWTH Aachen - URL: https://www.ukaachen.de/kliniken-institute/klinik-fuer-diagnostische-und-interventionelle-radiologie/fuer-patienten/magnetresonanztomographie-mrt-kernspintomographie
- MRT (Kernspintomografie); pA Medien GmbH; 2024 (abgerufen am 18.07.2024) - URL: https://www.praktischarzt.de/untersuchungen/mrt/
- Magnetresonanztomographie (MRT); MSD Manual (2023) (abgerufen am 12.07.2024) - Autor: Mustafa A. Mafraji - URL: https://www.msdmanuals.com/de/profi/spezielle-fachgebiete/grundz%C3%BCge-der-radiologischen-bildgebung/magnetresonanztomographie-mrt
- Infothek Radiologie: Mehr wissen über… Was klopft im MRT?; 2013 (abgerufen am 11.07.2024) - Autor: Taupitz, Matthias - URL: https://radiologie.charite.de/fileadmin/user_upload/microsites/m_cc06/radiologie/Radiologie/Durchblick/2013_Februar/Taupitz_022013.pdf
- Gadolinium-haltige Kontrastmittel: Aktualisierte Empfehlungen nach Bewertung von Gadoliniumablagerungen im Gehirn und anderen Geweben; 2018; (abgerufen am 17.07.2024) - Autor: Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) - URL: https://www.bfarm.de/SharedDocs/Risikoinformationen/Pharmakovigilanz/DE/RHB/2018/rhb-gadolinium.pdf?__blob=publicationFile&v=2
- Praxishandbuch Schlaganfall, 1. Auflage - Autoren: Kraft, Peter; Köhrmann, Martin - Publikation: Urban & Fischer Verlag/ Elsevier GmbH 2020
- Diffusion weighted imaging: Technique and applications; 2016 - Autoren: Baliyan, Vinit; Das, Chandan J.; Sharma, Raju; Gupta, Arun Kumar - Publikation: World Journal of Radiology, Bd. 8, Nr. 9, 2016, S. 785 - DOI: 10.4329/wjr.v8.i9.785
- Magnetic Resonance Imaging: Principles and Techniques: Lessons for Clinicians; 2015 - Autoren: Grover, Vijay P. B.; Tognarelli, Joshua M.; Crossey, Mary M. E., Cox, I. Jane; Taylor-Robinson, Simon D.; McPhail, Mark J. W. - Publikation: J Clin Exp Hepatol. 2015 Sep;5(3):246-55 - DOI: 10.1016/j.jceh.2015.08.001
- Identification of Potential Biomarkers for Patients with DWI-Negative Ischemic Stroke; 2024 - Autoren: Li, Lei; Wang, Ying - Publikation: Journal of Molecular Neuroscience, Bd. 74, Nr. 3, 2024, S. 68 - DOI: 10.1007/s12031-024-02229-z
- Ultrafast Brain MRI with Deep Learning Reconstruction for Suspected Acute Ischemic Stroke; 2024 - Autoren: Altmann, Sebastian; Grauhan, Nils F.; Brockstedt, Mariya Kondova; Schmidtmann, Irene; Paul, Roman; Clifford, Bryan; Feiweier, Thorsten; Hosseini, Zahra; Uphaus, Timo; Groppa, Sergiu; Brockmann, Marc A.; Othman, Ahmed E. - Publikation: Radiology. 2024 Feb;310(2):e231938 - DOI: 10.1148/radiol.231938
- Whole-body magnetic resonance imaging at 0.05 Tesla; 2024 - Autoren: Zhao, Yujiao; Ding, Ye; Lau, Vick; Man, Christopher; Su, Shi; Xiao, Linfang; Leong, Alex T. L.; Wu, Ed X. - Publikation: Science. 2024 May 10;384(6696):eadm7168 - DOI: 10.1126/science.adm7168
- Imaging bioluminescence by detecting localized haemodynamic contrast from photosensitized vasculature; 2024 - Autoren: Ohlendorf, Robert; Li, Nan; Phi Van, Valerie Doan; Schwalm, Miriam; Ke, Yuting; Dawson, Miranda; Jiang, Ying; Das, Sayani; Stallings, Brenna; Zheng, Wen Ting; Jasanoff, Alan - Publikation: Nat Biomed Eng. 2024 Jun;8(6):775-786 - DOI: 10.1038/s41551-024-01210-w
- Computertomographie; pA Medien GmbH; 2024 (abgerufen am 04.07.2024) - URL: https://www.praktischarzt.de/untersuchungen/computertomographie/
- High-Field Optical Cesium Magnetometer for Magnetic Resonance Imaging; 2024 - Autoren: Stærkind, Hans; Jensen, Kasper; Müller, Jörg H.; Boer, Vincent O., Polzik, Eugene S.; Petersen, Esben T. - Publikation: PRX Quantum 2024 Apr; Vol.5, Iss. 2 - URL: https://journals.aps.org/prxquantum/abstract/10.1103/PRXQuantum.5.020320
- 11.7 Tesla: First images from the world’s most powerful MRI scanner; 2024 (abgerufen am 18.07.2024); mgo Fachverlage GmbH & Co. KG - URL: https://healthcare-in-europe.com/en/news/11-7-tesla-first-images-world-most-powerful-mri-scanner.html